Introducción
La CU es una enfermedad crónica de origen autoinmune que cursa a modo de brotes de forma recurrente. Un 15% de los brotes serán cuadros graves que requieran ingreso con corticoides intravenosos[1], pudiendo presentar corticorresistencia hasta el 30% de estos pacientes. Se define CU grave (según los criterios de Truelove y Witts, figura 1) como aquella con más de 6 deposiciones con sangre al día, temperatura > 37.8 ºC, pulso > 90 lpm, hemoglobina < 10.5 g/dl y VSG> 30 mm/h[2]. El tratamiento de elección del brote grave de CU es con corticoterapia intravenosa a dosis de 1 mg/kg peso/día, con una tasa de respuesta del 50 al 70% en los primeros 5-7 días. En vista a estos datos se estableció una primera definición de CU corticorrefractaria como la falta de respuesta a dosis plena de corticoides intravenosos entre los días 5 al 10 de inicio del tratamiento[3]. Con el paso de los años se ha ido reduciendo el tiempo de espera para considerar fracaso del tratamiento, influenciado en parte por la gravedad del cuadro y en parte por la introducción de nuevos tratamientos, así han ido surgiendo numerosos estudios que intentan predecir la corticorresistencia al tercer día en función de parámetros como el número de deposiciones o la PCR. De entre ellos, en un estudio de 1996 se determinó que nos encontramos ante un fracaso terapéutico cuando al tercer día de tratamiento con corticoides iv a dosis plena el paciente presenta más de ocho deposiciones al día o tiene una PCR mayor de 45 mg/l, con un valor predictivo positivo del 85% para colectomía[4]. En otro estudio más reciente se revisaron los predictores clínicos de fracaso del tratamiento médico al tercer día, determinando que los más repetidos fueron la frecuencia de las deposiciones (más de 12 deposiciones al día en el segundo día de tratamiento tiene un riesgo de colectomía del 55% mientras que aquellos con más de 8 deposiciones al día tienen un riesgo del 85%), la temperatura, la frecuencia cardíaca, los niveles de PCR (PCR mayor de 45 mg/l en el día 3 asociada a un nº de deposiciones entre 3 y 8 se relaciona con un riesgo de colectomía del 85%), la albúmina < 3,0 g/dl, los niveles elevados de calprotectina fecal (> 1922 ug/g), una dilatación colónica > 5,5 cm en radiografía de abdomen (riesgo de colectomía del 75%) y la presencia de úlceras profundas en la colonoscopia (riesgo de colectomía del 93%)[5]. El estudio de estos marcadores provee a los especialistas de herramientas para identificar el fracaso terapéutico y considerar el uso de algún agente alternativo.
En general se recomienda iniciar terapia de "rescate" en pacientes con CU severa que no hayan respondido a tratamiento inicial con corticoides intravenosos después de 3 días de tratamiento. En caso de respuesta parcial al tercer día se podría esperar hasta 5-7 días antes de iniciar terapia de rescate. Además, como hemos mencionado, han de tenerse en cuenta los factores de riesgo anteriormente descritos y, en su presencia, dialogar con el paciente y su familia la posibilidad de un manejo futuro con infliximab o ciclosporina, e incluso también con el coloproctólogo ante el alto riesgo asociado de colectomía. Son varios los estudios que han evaluado la tasa de colectomía; según el grupo Oxford, el 28% de los pacientes que ingresaron por CU refractaria al tratamiento tenían una tasa de colectomía del 19.9% en el primer ingreso y del 40% después de 2 ingresos. Otro estudio del mismo grupo, demostró que cuando la respuesta al tratamiento médico es completa las tasas de colectomía a 1 y 5 años es de 5 y 32% respectivamente, mientras que con respuesta incompleta las tasas son de 51 y 77%[6]. Con respecto a la mortalidad a pesar del tratamiento adecuado la edad avanzada constituye un factor de riesgo como pudo objetivarse en un estudio de Travis y col. donde se observó que la mortalidad dependía de la edad, así en pacientes > 65 años era del 39% y en pacientes < de 30 años era del 0% a 3 años de seguimiento[7].
Manejo de la colitis ulcerosa grave
Una vez que nos encontramos ante un caso de CU severa debemos de abordarla de forma multidisciplinar con apoyo del intensivista y del coloproctólogo de forma precoz.
Pruebas diagnósticas
Su diagnóstico incluye solicitar análisis completo de laboratorio con hemograma, coagulación, bioquímica con pruebas de función renal e iones, VSG, PCR, albúmina, gasometría arterial, coprocultivo con estudio de parásitos y toxina A y B para Clostridium difficile así como hemocultivos si sospechamos infección.
Entre las pruebas de imagen a solicitar destacan la radiografía de abdomen simple para descartar dilatación colónica (megacolon tóxico) y radiografía de tórax y prueba de tuberculina para descartar tuberculosis latente ante la posibilidad de utilizar terapia biológica con anti-TNF[8].
La rectosigmoidoscopia es la prueba de elección para valorar la activad inflamatoria con toma de biopsias para estudio histológico y para descartar infección por citomegalovirus (en particular en pacientes expuestos previamente a corticoides o azatioprina)[9]. Es preferible evitar la realización de una colonoscopia total por el alto riesgo de perforación en esta situación.
Entre las infecciones oportunistas en los últimos años ha habido un aumento sobre todo de infección por Clostridium difficile, cuya toxina provoca en los pacientes con EII un curso más agresivo y severo, comparado con población general, tanto en niños como en adultos. La prevalencia de esta infección en pacientes con EII en brote oscila entre el 5-18% de los casos, siendo factores de riesgo la exposición previa a antibióticos, el uso de inmunosupresores (OR: 2,58), el uso previo de inhibidores de la bomba de protones, la edad avanzada, comorbilidades del paciente y la contaminación persona a persona. Su diagnóstico se realiza mediante la detección en heces de sus toxinas A y B con técnicas de ELISA. En caso de ser negativas en la toma inicial y ante la sospecha de su infección, la repetición de la misma incrementa la sensibilidad de la prueba. La infección por Clostridium difficile aumenta el tiempo de hospitalización y el riesgo de colectomía (OR: 6,6). Actualmente se recomienda que ante una alta sospecha de infección por Clostridium difficile en pacientes con EII con actividad severa y en presencia de factores de riesgo se solicite prueba de ELISA para toxinas A y B en materia fecal con el fin de obtener un diagnóstico y un tratamiento precoz y prevenir complicaciones tan severas como el megacolon tóxico y la necesidad de colectomía.
Manejo terapéutico
Debemos realizar un manejo terapéutico intensivo valorando en todo momento la situación clínica y evolución del paciente. Como tratamiento específico se recomienda:
Administrar un adecuado soporte de líquidos intravenosos (con una suplementación del potasio hasta obtener una diuresis > 50 cc/hora).
Transfusión de sangre si es preciso para mantener una Hb > 10 g/dl.
Suspensión de antidiarreicos, anticolinérgicos, AINES y opioides en caso de que el paciente los estuviera tomando.
Realizar profilaxis de trombosis venosa mediante heparinas de bajo peso en aquellos pacientes que tengan factores de riesgo de fenómenos tromboembólicos. Es importante señalar que los pacientes con EII tienen tres veces más riesgo de presentar eventos tromboembólicos (incidencia de 1-6,7%), con predominio de trombosis venosa profunda y tromboembolismo pulmonar comparados con la población general, con mayor tendencia a presentarse en edades más tempranas[12]. Este estado procoagulante se debe a factores protrombóticos tanto congénitos como adquiridos. Entre los factores heredados los más frecuentes son la mutación del factor V de Leiden, la mutación homocigótica C667T del gen de la metil entetrahidrofolatorreductasa y la mutación del gen 20210A de la protrombina. Entre los factores adquiridos están el tabaco, el estado inflamatorio, la inmovilización prolongada, la hiperhomocisteinemia (secundaria a déficits nutricionales de vitamina B12, vitamina B6 y de ácido fólico), la cirugía, el uso de catéteres venosos centrales, el tratamiento con corticoides o el uso de anticonceptivos orales.
Tratamiento con corticoides intravenosos a dosis plena (1 mg/kg peso/día). A los pacientes que no respondan a corticoides intravenosos al tercer día de admisión se les debe ofrecer terapia de "rescate" con infliximab a dosis de 5 mg/kg de peso (en inducción en las semanas 0,2 y 6 y de mantenimiento cada 8 semanas) o ciclosporina a dosis de 2 mg/kg de peso/día.
Todos los pacientes deben ser valorados por un cirujano dado el alto riesgo de colectomía. En general el 6-7,9% de los pacientes con CU severa desarrollarán megacolon tóxico, con una tasa de mortalidad del 19% aproximadamente y de hasta el 42% en caso de que se asocie con perforación colónica. En el manejo de estos individuos existen tres grandes dilemas (cómo identificar pacientes de alto riesgo para complicaciones, cuándo iniciar terapia de rescate con infliximab o ciclosporina y cuándo tomar la decisión oportuna de realizar colectomía).
Ciclosporina A
La ciclosporina A es un péptido cíclico inhibidor de la calcineurina extraído del hongo Tolypocladium inflantum que actúa bloqueando de forma directa la proliferación de linfocitos T. Su uso en la medicina se introdujo en 1978 y durante muchos años previos a la introducción del infliximab ha supuesto la única alternativa a la proctocolectomía en los pacientes con CU grave refractaria a corticoides.
Desde la publicación de Lichtiger y col. de un estudio que comparaba ciclosporina con placebo son numerosos los estudios retrospectivos y series de pacientes que han corroborado la eficacia de ciclosporina en el brote grave de CU refractaria a corticoides, aunque sólo se dispone de tres estudios publicados aleatorizados acerca de su eficacia en la CU refractaria al tratamiento corticoideo. El resto de estudios que existen presentan defectos de forma (estudios abiertos, estudios no aleatorizados, etc).
En el estudio de Lichtiger y col. se aleatorizaron a 20 pacientes con CU grave refractaria (falta de respuesta a al menos 7 días con corticoides iv. a dosis plena) en dos grupos, el grupo tratado con ciclosporina (4 mg/kg/día de ciclosporina en infusión continua) frente al grupo placebo[11]. Se consideró respuesta al tratamiento cuando la puntuación de actividad clínica disminuía al menos 10 puntos (promedio al inicio de 13) en dos días consecutivos. Se logró respuesta en el 82% de los pacientes tratados con ciclosporina frente al 0% en el grupo placebo con una tasa de colectomía del 18% en el grupo de tratamiento con ciclosporina frente a un 44% en el grupo placebo. El segundo estudio del que disponemos fue el realizado por D’Haens y col., que incluyó 30 pacientes con CU grave que fueron aleatorizados a recibir durante 8 días ciclosporina iv. (4 mg/kg/día) frente a metilprednisolona intravenosa (40 mg/día)[12]. La tasa de respuesta fue del 64% en los pacientes tratados con ciclosporina (con remisión mantenida al año en el 78%) frente al 53% de los que recibieron metilprednisolona. El tercer estudio disponible es el de Van Assche y col. donde se compararon 4 mg/kg/día de ciclosporina intravenosa frente a 2 mg/kg/día[13] observando que la eficacia de la ciclosporina a dosis inferiores (2 mg/kg/día) es igual que la considerada como estándar (4 mg/kg/día) pero con menor frecuencia de efectos adversos, aunque la dosis final siempre debe ajustarse a los niveles plasmáticos del fármaco (150-250 ng/ml) y a la coexistencia de efectos adversos.
Monitorización del tratamiento con ciclosporina
Con respecto a los niveles plasmáticos de la ciclosporina, el objetivo es obtener niveles en sangre entre 60 y 600 ng/ml (determinados por radioinmunoensayo con un anticuerpo monoclonal). Dicha monitorización de sus niveles plasmáticos se debe realizar a partir de las dos horas de la administración del fármaco en lugar de la monitorización del nivel valle. En los tres estudios arriba mencionados los niveles medio de ciclosporina en sangre estuvieron entre 350-450 ng/ml con dosis de 4 mg/kg peso/día y de 237 ng/ml con dosis de 2 mg/kg peso/día, pero no se halló una correlación entre los niveles de la ciclosporina y la respuesta clínica. En vista a estos datos se recomienda en la práctica alcanzar unos niveles de ciclosporina en sangre de 150 a 250 ng/ml[14]. Se desconoce si niveles menores tendrían efectos iniciales similares.
Perfil de seguridad de la ciclosporina
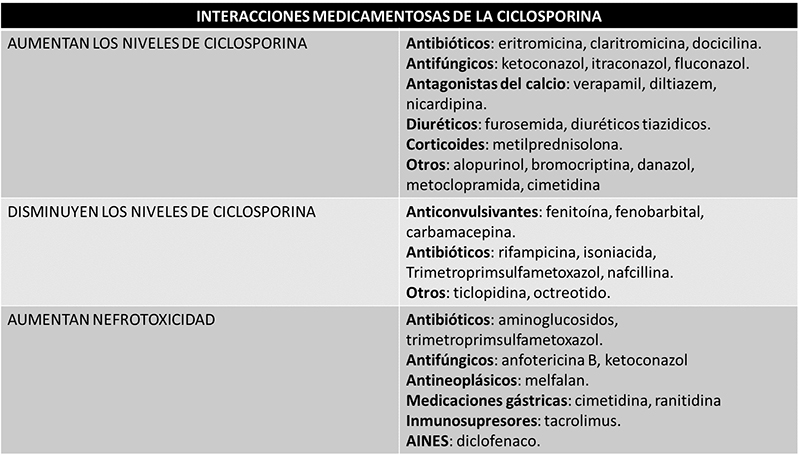
El perfil de seguridad de ciclosporina es bien conocido. Antes de optar por el tratamiento con ciclosporina es importante evaluar los siguientes factores: riesgo de enfermedad renal (edad >50 años, hipertensión arterial, diabetes mellitus), historia personal de neoplasias, infecciones activas, medicaciones concomitantes con las que puede haber interacciones farmacológicas (Figura 2) y embarazo. En la práctica clínica, durante el tratamiento con ciclosporina debe monitorizarse la presión arterial, realizar análisis de sangre seriados (electrolitos, creatinina, niveles de colesterol y de magnesio, pruebas de función hepática) y medir regularmente los niveles de fármaco en sangre como ya hemos mencionado. En un 20% de los pacientes tratados con ciclosporina ocurren eventos adversos, siendo más frecuente en los tratados con dosis altas intravenosas[15]. Entre los efectos adversos más importantes destacan las infecciones oportunistas, seguidas de la nefrotoxicidad y neurotoxicidad. El riesgo de infecciones oportunistas (Pneumocystis carinii, Nocardia, Aspergillus fumigatus, Listeria meningitidis, Citomegalovirus, Herpes simple, Candida, sepsis por Staphylococcus o Haemophilus influenza) se ha descrito casi siempre en relación con la dosis y también con el uso concomitante de fármacos inmunosupresores; la insuficiencia renal leve es relativamente frecuente y debida a una vasoconstricción dosis-dependiente de las arteriolas aferentes y eferentes. La insuficiencia renal grave es mucho menos frecuente; los efectos secundarios neurológicos varían entre síntomas leves (temblor, parestesias, cefalea) hasta síntomas más graves (convulsiones). Dicha neurotoxicidad es más frecuente en pacientes tratados con ciclosporina iv. y con niveles bajos de colesterol (menor a 100 mg/dL) o de magnesio. Otros efectos adversos de menor gravedad o baja frecuencia incluyen: hirsutismo, temblores, hiperplasia gingival, cefaleas o alteraciones de pruebas de función hepática (elevación de transaminasas en sangre). No se ha comunicado el desarrollo de neoplasias en CU secundarias al tratamiento con ciclosporina.
Al hablar del perfil de seguridad de la ciclosporina no podemos dejar atrás mencionar la existencia de la ciclosporina oral en microemulsión, que ha demostrado en varios estudios una eficacia similar a la ciclosporina iv. en el brote grave de CU, así Navazo y col. obtuvieron unas tasas de respuesta temprana del 70-90% y una tasa de enfermedad libre de colectomía del 47-74% usando ciclosporina oral a dosis de 8 mg/día[16]. Aunque los resultados fueron similares se ha demostrado que el grupo tratado con ciclosporina iv. tenía una mayor tasa de toxicidad (17%), incluyendo la muerte. Por otro lado, en un estudio controlado D’Haens y col. se demostró que la ciclosporina en monoterapia es tan eficaz como los corticoides para inducir la remisión del brote grave de CU, por lo que se podría plantear que en situaciones donde no se pueda administrar corticoides (contraindicación, antecedentes de efectos adversos graves con la toma de corticoides como brotes psicóticos, o situaciones que desaconsejen el uso de corticoides, como en el caso de osteoporosis grave), la ciclosporina en monoterapia constituye una opción terapéutica adecuada para inducir la remisión[17].
Tratamiento de mantenimiento una vez alcanzada la remisión con ciclosporina
Aunque la ciclosporina pueda ser útil para inducir la remisión, no lo es en monoterapia para el mantenimiento de la remisión, por lo que es necesario asociarle otros fármacos. Se han propuesto dos alternativas, una es la asociación de azatioprina a dosis de 2-2,5mg/kg/día o 6-mercaptopurina a dosis de1-1,5mg/kg/día, corticoides en pauta descendente hasta su suspensión completa y ciclosporina oral (ésta última debe suspenderse a los 3-6 meses debido a sus efectos adversos, principalmente la neurotoxicidad, que puede ser irreversible). Diversos estudios han demostrado que la tasa de pacientes libres de colectomía fue mayor en aquellos pacientes que recibieron azatioprina/6MP (80%) frente a los que no (55%), lo que demuestra la importancia del pasaje a azatioprina/6MP. El problema de esta pauta con triple inmunosupresión es el aumento del riesgo de infecciones que obliga a mantener tratamiento profiláctico con trimetropim-sulfametoxazol para evitar la sobreinfección por Pneumocystis carinii. Surge así la segunda opción terapéutica, defendida por otros autores y que no incluye la ciclosporina oral, con lo que se evitan sus posibles efectos secundarios y disminuye el riesgo de infecciones oportunistas. En esta pauta de tratamiento se utiliza la ciclosporina iv. durante un corto periodo de tiempo (días), sólo para inducir remisión, y se inicia inmediatamente después tratamiento con azatioprina y pauta descendente de corticoides. En esta línea se encuentra el estudio de Domenech y col., donde de forma no controlada evalúan la respuesta a dicho tratamiento en 27 pacientes concluyendo que la azatioprina es eficaz y segura en el mantenimiento de la remisión de los pacientes con brote severo corticorrefractario de CU controlados con ciclosporina iv., no siendo necesario el tratamiento puente con ciclosporina oral[18]. No obstante, son necesarios estudios controlados y randomizados para confirmar si es adecuada o no la estrategia de doble inmunosupresión comparada con la estrategia de triple inmunosupresión.
Resultados a largo plazo tras tratamiento con ciclosporina
Evaluando la necesidad de colectomía, Cohen y col. observaron que el 72% de los pacientes que respondieron a la ciclosporina evitaron la colectomía 5.5 años del tratamiento[19], sin embargo, el 51% de los pacientes del estudio de Lichtiger que no respondieron (bien a la remisión del brote con ciclosporina oral o bien al tratamiento de mantenimiento con ciclosporina oral y/o azatioprina/6MP) fueron sometidos a colectomía a los 2 años[20]. Diversos estudios han observado también que la tasa de colectomía disminuye si se añade azatioprina/6MP como mantenimiento una vez conseguida la respuesta a la ciclosporina oral (tasa libre de colectomía del 80% en pacientes tratados con azatioprina/6MP frente a un 55% en los no tratados como mantenimiento)[21]. Sin embargo, la tasa de colectomía se duplicaba si el paciente tomaba previamente al brote azatioprina/6MP (del 31 al 59%), lo que implica que en los sujetos con brote de CU severa refractaria a corticoides que estaban tomando azatioprina/6MP el tratamiento de elección no debe ser la ciclosporina. Para terminar existe un estudio independiente llevado a cabo por Cohen y col. que demuestra que los pacientes que fueron tratados con ciclosporina y que obtuvieron buena respuesta evitaron la colectomía y presentaron menos tasas de síntomas intestinales y menos ingresos hospitalarios[22].
En resumen, la ciclosporina resulta ser un fármaco seguro y efectivo para lograr una respuesta clínica en los pacientes con CU grave que fracasaron al tratamiento con corticoides intravenosos con el fin de evitar la colectomía. El uso de ciclosporina en dosis bajas intravenosas o por vía oral es probablemente más eficaz y menos tóxica que las dosis mayores. Quienes responden a la ciclosporina deben pasar a azatioprina/6MP a medio/largo plazo. Como limitación al uso de ciclosporina, están sus efectos secundarios, su falta de respuesta en pacientes inmunodeprimidos y la necesidad de determinar sus niveles en sangre así como los niveles de magnesio y colesterol en sangre. Si se opta por el tratamiento con ciclosporina es muy importante evaluar la eficacia de la ciclosporina de forma precoz y, en ausencia de respuesta clínica en 3-5 días de tratamiento, debe de plantearse otra alternativa, ya sea médica o quirúrgica. En caso de que sí exista respuesta a la ciclosporina iv. al cabo de estos 3-5 días se debe de iniciar tratamiento con ciclosporina vía oral 5-8 mg/Kg dividido en dos dosis (durante 3 semanas-3 meses) e ir reduciendo la dosis de corticoides al tiempo que se añade el tratamiento con azatioprina/6-MP.
Infliximab
El infliximab es un anticuerpo monoclonal quimérico (75% humano, 25% ratón) de la clase IgG-1 que actúa contra el factor de necrosis tumoral α (citoquina de respuesta tipo TH-1 que posee una intensa acción pro-inflamatoria) Ha sido utilizado durante años para el tratamiento de la enfermedad de Crohn. Su papel en la CU se basa en una disminución de los efectos del TNF-α y de su cascada inflamatoria en la mucosa colónica que en los últimos años lo ha situado en la escala terapéutica de la CU, siendo eficaz en inducir y mantener la remisión así como en disminuir la tasa de colectomía en pacientes con CU refractaria a corticoides. Para entender el papel del infliximab en el brote de CU sería interesante mencionar el rol del factor de necrosis tumoral α (TNF-α) en la CU. Los primeros estudios a este respecto mostraron que los pacientes con CU no presentaban niveles elevados de este factor, sin embargo estudios posteriores han puesto de manifiesto que de los niveles de TNF-α dependerá la severidad del cuadro clínico, endoscópico e histológico. Así se ha observado que en pacientes con CU grave, los niveles de TNF-α son significativamente más elevados que en los individuos sin colitis y en los pacientes con CU en etapa de remisión o con actividad leve a moderada.
IFX ha demostrado una eficacia con alto nivel de evidencia en inducir y mantener la remisión en CU de moderada a grave refractaria al tratamiento con corticoides o incluso con inmunomoduladores. Asimismo es eficaz en conseguir la cicatrización mucosa y disminuir la necesidad de colectomía. La mayoría de los estudios controlados sobre la eficacia de infliximab en la CU se han realizado en pacientes con CU refractaria a los corticoides. En uno de ellos Sands y col. seleccionaron 11 pacientes con CU refractaria (tras cinco días con corticoides iv. a dosis plena) a recibir de forma aleatoria infliximab versus placebo[23]. La respuesta clínica a las dos semanas fue del 50% en los pacientes tratados con infliximab frente al 0% en los pacientes tratados con placebo. En esta línea Janerot y col. evaluaron la utilidad de una sola infusión de infliximab en pacientes con CU refractaria al cuarto día de tratamiento corticoideo (CU fulminante) o al 6-8 día de tratamiento (CU grave). De los 45 pacientes seleccionados, el 29% precisó de colectomía a los 3 meses, en comparación con el 67% de los que recibieron placebo (p = 0.017), con un beneficio más definido para el grupo con enfermedad grave que para el grupo con enfermedad fulminante. Rutgeerts y col. publicaron los resultados de dos estudios controlados (ACT-1, ACT-2) con más de 700 pacientes con CU moderada a grave, de los cuales 217 casos fueron CU refractaria a corticoides (tras siete días de no respuesta a dosis plena de prednisona o tras catorce días de no respuesta a dosis de 40 mg de prednisona oral) consiguiendo una tasa de respuesta clínica temprana del 63-77%. Entre otros estudios sobre infliximab en el tratamiento de la CU refractaria a corticoides en pacientes tratados con azatioprina/6MP destaca el llevado a cabo en 2004 por Mamula y col. en el que comparaban la tasa de respuesta en pacientes con CU en los que hubo fracaso tras tratamiento previo con azatioprina/6MP y pacientes naive para azatioprina/6MP, obteniendo una tasa de respuesta similar en ambos grupos (80%). La importancia de este estudio radica en que el infliximab, a diferencia de la ciclosporina, podría ser una buena opción en aquellos pacientes con CU grave tratados con azatioprina/6MP en los que haya fracaso al tratamiento corticoideo[16].
Monitorización del tratamiento con Infliximab
Infliximab ofrece la ventaja, con respecto a ciclosporina, de que no precisa medir sus niveles en sangre para poder administrarlo en el paciente.
Su dosis de administración será de 5 mg/kg peso en las semanas 0,2, 6 en la inducción para luego ser cada 8 semanas de mantenimiento. Como ya sabemos es recomendable el tratamiento inmunomodulador concomitante con el fin de disminuir el riesgo de inmunogenicidad por la creación de anticuerpos anti-infliximab (relacionados con las reacciones infusionales y con la pérdida de eficacia del infliximab).
Perfil de seguridad del infliximab
Con respecto a su perfil de seguridad destacan las reacciones a la infusión, las infecciones y el riesgo de neoplasias.
Se cree que las reacciones a la infusión se deben al desarrollo de anticuerpos anti-infliximab (ATI), que ocurre en el 13-18% de los pacientes tratados. Dicha reacción infusional puede ser precoz o tardía. La precoz suele consistir en síntomas leves (enrojecimiento facial) aunque también graves (shock anafiláctico, disnea, hipotensión arterial).La disminución del ritmo de la infusión es, en la mayor parte de los casos, suficiente para tratar estos procesos y se pueden completar las infusiones, a pesar de haber aparecido la reacción, cuando son leves. También la asociación de inmunosupresores, la administración previa a la infusión de una dosis de hidrocortisona por vía intravenosa y el acortamiento del intervalo de tiempo transcurrido entre las infusiones pueden disminuir de forma notable tanto la frecuencia como la intensidad de las reacciones alérgicas secundarias a su administración.
Las reacciones tardías más frecuentes son la aparición de dolor e hinchazón a nivel de diferentes articulaciones (se tratan habitualmente con AINEs y/o corticoides).
En cuanto a la aparición de efectos adversos infecciosos, uno de los más importantes es el aumento del riesgo de tuberculosis, así, en una revisión efectuada sobre datos aportados por la FDA americana sobre un total de 150.000 pacientes tratados con IFX hasta el 29 de mayo del 2001, habían aparecido 70 casos de tuberculosis, con una media de 12 semanas de tratamiento, 40 de los cuales presentaban afectación extra-pulmonar, tratándose en la mayoría de los casos, de reactivaciones de una enfermedad latente, previamente existente.
Con respecto a la aparición de posibles neoplasias relacionadas con la toma del IFX, se desconoce si la administración a largo plazo es capaz de provocar un aumento en la incidencia de estos procesos malignos, tanto linfomas como tumores sólidos, por sus efectos inmunosupresores aumentados con el empleo simultáneo de otros fármacos (AZT o MTX), pero por el momento no parece estar incrementada y existe una amplia experiencia acumulada con la utilización del IFX.
Tratamiento de mantenimiento una vez alcanzada la remisión con Infliximab
Como ya hemos mencionado antes debe ser con infliximab a dosis de 5 mg/kg de peso cada 8 semanas, preferiblemente acompañado por otro inmunomodulador.
Resultados a largo plazo tras tratamiento con Infliximab
Como resultado a largo plazo se ha determinado en diversos estudios que la tasa total de colectomía en pacientes con CU refractaria a corticoides tratados con infliximab es del 30% al año y del 50% a los dos años[16], [20], datos que apoyan una reducción en la tasa de colectomía con el uso de infliximab.
En la actualidad disponemos de dos opciones terapéuticas de primera línea como son ciclosporina A e infliximab, teniendo en cuenta la limitación que ofrece el uso de ciclosporina tanto por requerir mediciones en sangre de sus niveles como de la contraproducencia de su uso en pacientes previamente tratados con azatioprina/6MP. Se han publicado varios estudios que intentar evidenciar si existen o no diferencias entre ambas opciones terapéuticas. En 2011 se realizó el primer estudio controlado, aleatorizado y multicéntrico que compara la respuesta de ciclosporina frente a infliximab en CU severa corticorrefractaria (Estudio CYSIF). Participaron un total de 111 pacientes que se aleatorizaron a dos grupos de tratamiento (55 pacientes a ciclosporina y 56 pacientes a infliximab). No se observaron diferencias significativas en cuanto a la respuesta, fracaso y tasas de colectomía en ambos grupos terapéuticos[24]. En 2012, Dean KE y col. han publicado un estudio retrospectivo en el que analizan las tasas de colectomía a los 3 y 12 meses en 37 pacientes con CU grave corticorrefractaria que iniciaron tratamiento con ciclosporina o infliximab. Observan un aumento de la tasa de colectomía en el grupo de ciclosporina frente a infliximab a los 3 meses (63% vs 21%) y también a los 12 meses (68% vs 37%)[25]. En 2013 se ha publicado un meta-análisis de 361 pacientes de 6 estudios de cohortes retrospectivas que concluyó que infliximab y ciclosporina son comparables cuando se utilizan como terapia de rescate en CU grave corticorrefractaria[26]. Recientemente se ha publicado el diseño y protocolo de un ensayo clínico, controlado y aleatorizado en el que se quiere comparar si existen diferencias entre ambas terapias en CU severa corticorrefractaria en cuanto a respuesta clínica y coste-efectividad de infliximab y ciclosporina en estos pacientes. Han participado 270 pacientes de 52 centros de Reino Unido aunque aún no se han publicado resultados[27].
Ante la necesidad de escoger entre ciclosporina e infliximab en la CU refractaria y el escaso número de estudios comparativos, se han buscado factores predictivos de respuesta a ambos fármacos, entre los factores clínicos y biológicos identificados como factores predictivos de fracaso a ciclosporina destacan la hipoalbuminemia, proteína C reactiva, fiebre y taquicardia, aunque el carácter retrospectivo de estos estudios limita su validez[28].
Terapia de Rescate de "segunda línea"
Una posible opción ante el fracaso a la ciclosporina (antes de recurrir a la colectomía) podría ser el infliximab administrado de forma secuencial. Sin embargo, uno de los principales inconvenientes de esta modalidad secuencial radica en el perfil de seguridad de esta asociación. La ciclosporina iv tiene una vida media en sangre de 6 horas[29] mientras que infliximab permanece en suero un mínimo de 8 semanas[30], por lo que parece razonable que se pueda iniciar infliximab tras ciclosporina pero no a la inversa. Algunos autores han realizado manejo secuencial con terapia de "rescate" con infliximab y luego ciclosporina o viceversa, así Maser evaluó en 2003 de forma retrospectiva[31] la eficacia a infliximab en 19 pacientes con CU corticorrefractaria postciclosporina (n=10) o viceversa (n=9), logrando remisión clínica en 3 meses en el 40% de los pacientes que fueron tratados con infliximab tras no obtener respuesta inicial con ciclosporina y en el 33% de los pacientes tratados con ciclosporina que previamente no obtuvieron respuesta al infliximab, sin embargo la tasa de colectomía tras 2 meses de tratamiento con infliximab fue del 40% y sólo en un 37% de los casos se consiguió retirar los corticoides, además el riesgo de eventos adversos aumentó al 16% incluyendo una muerte (secundaria a sepsis por gram negativos), una bacteriemia en un paciente con pancreatitis y una esofagitis herpética. La tasa de colectomía total al año fue del 42%. Un reciente estudio del grupo francés GETAID con una serie más amplia, de 87 pacientes, evaluó también la eficacia de la terapia secuencial. En este estudio el 30% de los pacientes fueron colectomizados a los tres meses de tratamiento con una tasa acumulada de colectomía al año del 46%. La tasa de remisión fue del 22% a los 3 meses de seguimiento con un 16% de complicaciones infecciosas (sepsis, absceso postoperatorio, sobreinfección por citomegalovirus, diarrea por Clostridium difficile, neumonía y absceso hepático) con una muerte por tromboembolismo pulmonar[32]. También recientemente se ha publicado un estudio retrospectivo, multicéntrico y español que analiza el rescate con infliximab en aquellos pacientes con CU severa corticorrefractaria que han fracasado a ciclosporina. Se analizaron un total de 47 pacientes con un índice medio de Lichtiger de 13 y cuyo tiempo medio desde la última dosis de ciclosporina a la primera infusión de infliximab fueron 6 días. Tras la primera infusión de infliximab el 13% alcanzó la remisión y un 74% una respuesta parcial. De los 35 pacientes que recibieron la 3ª dosis de infliximab, el 60% alcanzó la remisión. 14 pacientes (30%) fueron sometidos a colectomía. El 23% presentó algún evento adverso y hubo un paciente que falleció tras fracasar a infliximab y realizarse colectomía 10 días tras primera infusión. Concluyen que el tratamiento con infliximab puede evitar la colectomía hasta en dos tercios de los pacientes con CU corticorresistente refractarios a ciclosporina aunque la tasa de eventos adversos y la mortalidad implicarían que la decisión de administrar la terapia secuencial (ciclosporina-infliximab) debe tomarse de forma individual[33]. Este año se ha publicado una revisión sobre estudios que valoran la respuesta de esta terapia secuencial. Analizaron 10 estudio con un total de 314 pacientes observándose que tras el tratamiento secuencial alcanzan la respuesta a corto plazo el 62.4% de los casos y remisión el 38.9%. Las tasas de colectomía fueron de 28.3% a los 3 meses y 42.3% a los 12 meses. Hasta un 23 % de los pacientes presentaron algún evento adverso (6.7% infecciones graves y 1% mortalidad)[34].
De lo anterior se deduce que realizar tratamiento de "rescate" de segunda línea es menos efectivo y seguro comparándolo con la terapia de primera línea, quedando la colectomía como opción de tratamiento en los que falla el tratamiento médico de rescate o bien usar infliximab en una cohorte de pacientes muy seleccionada en los que se pueda evitar la colectomía, con especial atención al desarrollo de complicaciones infecciosas (sería aconsejable usar medidas preventivas para Pneumocystis jiroveci con cotrimoxazol y de infecciones latentes como la tuberculosis).
Cabe la duda del resultado que obtendríamos al tratar con ciclosporina a pacientes en los que haya fracasado el uso de infliximab. En este sentido Maser y col. informaron que 3/9 (33%) de los pacientes lograron la remisión con ciclosporina luego del fracaso con infliximab con un riesgo de eventos adversos del 16%[35]. Por el contrario, Manosa y col. señalaron que 6/13 (46%) de los tratados con infliximab tras el fracaso con ciclosporina necesitaron colectomía a los 6 meses[36].
Con respecto al riesgo de infecciones oportunistas podemos afirmar que aumenta en sentido ascendente en los tratados con corticoides, ciclosporina e infliximab. Así Yang Z. y col. demostraron en un meta análisis que el riesgo de infección poscolectomía esta mayor en pacientes que han recibido infliximab con una odds ratio de 2,24[37].
Nuevas terapias médicas
Existen algunos estudios no controlados donde se han usado otros inmunosupresores como la ciclofosfamida en pulsos, la aféresis por absorción selectiva de leucocitos, el adalimumabYO NO METERÍA AQUI AL ADALIMUMAB (agente anti-TNF-α, el golimumab (agente anti-TNF-α), el basiliximab (anticuerpo monoclonal quimérico murino/humano que actúa contra la cadena α del receptor de la interleukina-2) y el vedolizumab (anticuerpo monoclonal humanizado de tipo IgG1 que se une a la integrina α4β7 humana), el tacrolimus, la talidomida, el interferón natural β y la fosfatidilcolina. Ninguno se ha posicionado como una terapia tradicional fuera del ámbito de los estudios clínicos o con expertos locales. Valoraremos a continuación los más conocidos.
Aféresis
La aféresis consiste en la extracción selectiva de los leucocitos circulantes activados mediante un sistema extracorpóreo, produciendo el paso de leucocitos no activados al torrente circulatorio provocando un fenómeno de inmunomodulación[38]. Esta técnica ofrece las ventajas de ser bien tolerada y de provocar escasos efectos adversos. Sin embargo los diversos estudios publicados sobre su eficacia en la CU presentan gran heterogeneidad en las definiciones de corticorrefractariedad, corticodependencia, remisión y eficacia utilizadas, en la pauta del esquema terapéutico y en las poblaciones estudiadas lo que no nos permiten extrapolar. Se podría platear realizar estudios no heterogéneos que permitan obtener la suficiente evidencia científica como para poder plantear la aféresis como alternativa a la colectomía ante falta de respuesta a la terapia de rescate (ciclosporina o infliximab), pero en la actualidad la aféresis sólo se aconseja como tratamiento de segunda línea o de rescate en los casos de brotes no graves de CU.
Tacrólimus
El tacrolimus es un macrólido aislado del Streptomices tsukubaensis descubierto en 1984 por Fujisawa Pharmaceutical Co. con un mecanismo de acción similar a la ciclosporina pero una potencia inmunosupresora de 10-100 veces superior, una absorción intestinal rápida no dependiente de la integridad de la mucosa intestinal y con gran variabilidad individual que obliga a un estrecho seguimiento de los valores plasmáticos del fármaco (intervalo terapéutico 4-10 ng/mL) (41).La principal fuente de información sobre su efecto inmunosupresor proviene de su uso en el trasplante renal y hepático[39]. La evidencia científica en EII es escasa debido al tamaño y heterogeneidad de los estudios siendo necesarios estudios randomizados para establecer su eficacia en estas situaciones[40], [41] .
Basiliximab y visilizumab
El basiliximab es un anticuerpo monoclonal con afinidad por la subunidad α del receptor de la interleucina 2 de los linfocitos T (también llamada antígeno CD25), usado durante años en la enfermedad injerto contra huésped y en el trasplante de órganos sólidos. Recientes estudios en adultos y niños sugieren que la terapia con anti-CD25 podría restablecer la sensibilidad a corticoides de las células T en la CU corticorresistente y corticodependiente. Su uso podría estar restringido a la inducción de una respuesta transitoria en los pacientes con CU fulminante que no respondan a los tratamientos habituales para realizar un abordaje quirúrgico diferido que disminuya la morbimortalidad[42], [43].
El visilizumab es un anticuerpo monoclonal contra el CD3, también en investigación para el tratamiento de la CU grave refractaria a corticoides con una eficacia modesta y frecuentes efectos colaterales[44].
Golimumab
Golimumab es un anticuerpo monoclonal humano que impide la unión del TNF-α a sus receptores mediante la formación de complejos estables por su gran afinidad con las dos formas bioactivas del TNF-α humano, la soluble y la transmembranosa. Su eficacia para inducir remisión en inducción y mantenimiento ha sido demostrada en los estudios PURSUIT-SC y PURSUIT-M. Comparado con los otros dos antiTNF más conocidos, Infliximab y Adalimumab, parece ser que golimumab posee mayor afinidad por la fracción soluble del TNF que adalimumab e infliximimab, y similar afinidad por el receptor transmembrana que infliximab, siendo superior a adalimumab. Respecto a la eficacia comparada, no existe suficiente evidencia para sugerir diferencias entre los tres fármacos anti-TNFα, Infliximab, adalimumab y golimumab, los tres se toleran bien y presentan un perfil de seguridad similar al del placebo. Tampoco existe suficiente evidencia para sugerir diferencias entre los tres fármacos en cuanto a seguridad. Con respecto al coste, resulta al menos igual o más eficiente que adalimumab e infliximab. Está aprobado por la FDA para el tratamiento de la CU activa de moderada a grave en pacientes adultos con respuesta inadecuada al tratamiento convencional, incluidos corticoides y 6-mercaptopurina (6-MP) o azatioprina (AZA), o que presentan intolerancia o contraindicaciones a dichos tratamientos. Su posología parece ser más cómoda para el paciente que adalimumab, pues sería de 200 mg (semana 0), 100 mg (semana 2) y 100 mg ó 50 mg c/ 4 semanas de mantenimiento.
No se dispone de estudios actualmente que valoren su eficacia en el tratamiento de la CU severa refractaria a corticoides.
Vedolizumab
Vedolizumab es un anticuerpo humanizado que inhibe la adhesión y la migración de los leucocitos a través del tracto gastrointestinal mediante el bloqueo de la interacción entre la subunidad α4β7 de las integrinas y la molécula de adhesión mucosal MadCAM-1 (adresina con expresión elevada en los vasos sanguíneos del tracto intestinal). La eficacia y seguridad de vedolizumab en la CU dos ensayos clínicos en los que se incluyeron un total de 900 pacientes que no habían respondido a tratamientos previos con corticoides, inmunomoduladores o inhibidores del TNF-α en los que se evaluaron la frecuencia de deposiciones, el sangrado rectal y las lesiones endoscópicas en pacientes con CU, mostrando, en comparación con placebo, que vedolizumab induce un mayor porcentaje de respuesta clínica y tasas de mantenimiento. El tratamiento también se asoció a mejoras histológicas en la mucosa del colon. Las principales ventajas de vedolizumab residen en su novedoso mecanismo de acción y en su gran selectividad por la mucosa intestinal. Quedan pendientes estudios que evalúen su eficacia en la CU severa refractaria a corticoides.
Adalimumab
En la actualidad no existen estudios que muestren la eficacia de adalimumab en el brote severo de CU. Los únicos datos que existen son sobre CU moderada y provienen de estudios observacionales a corto plazo o de presentaciones a congresos. El único ensayo clínico sobre adalimumab para la CU (y no severa, sino moderada a severa) es el realizado por Reinisch y col. en el que comparan adalimumab frente a placebo en más de 500 pacientes con CU moderada a severa sin respuesta o con intolerancia previa a corticoides o inmunomoduladores[45]. Se utilizaron 2 pautas diferentes de adalimumab para la inducción (160/80 y 80/40) y se evaluó la remisión clínica en la semana 8 siendo del 18,5% en el grupo tratado con adalimumab 160/80 (p = 0,031 versus placebo), del 10,0% en el grupo adalimumab 80/40 (p = 0,833 versus placebo) y del 9,2% en el grupo placebo. Adalimumab fue bien tolerado y muestra una eficacia estadísticamente significativa aunque sólo discretamente superior a placebo y sólo para la dosis de 160/80, llamando la atención la alta respuesta obtenida con placebo. Son necesarios más estudios sobre adalimumab para la CU severa, puede que el incremento de la dosis de adalimumab pueda optimizar su eficacia.
Colectomía
Hoy en día la colectomía total o la colectomía subtotal con anastomosis ileorectal (AIR) sigue siendo la alternativa a usar ante fracaso del tratamiento médico o la aparición de complicaciones con una tasa de complicaciones tempranas menor al 10%, además de suponer la "curación" de la CU y prevenir del cáncer de colon. Dentro de estos dos tipos de procedimientos es la colectomía subtotal+AIR la más elegida tanto por el paciente (permite mantener el tránsito normal y evita la ileostomía definitiva) como por los mejores índices de calidad registrados tras la cirugía[46]. Sin embargo cabe resaltar que un 10% de estos pacientes sufrirá disfunción anal con incontinencia y requerirán finamente una ileostomía[47].
Así Cohen y col. que compararon a pacientes con CU grave que respondieron a ciclosporina frente a los que recibieron colectomía objetivando que los primeros tenían mejor calidad de sueño, mejor consistencia de sus heces, menos dolor abdominal o rectal, e iban al baño con menos frecuencia que los operados. Además de una probable merma en la calidad de vida la colectomía también se relaciona con una serie de complicaciones, como la pouchitis (la más frecuente, hasta en un 50% de los casos), la cuffitis, el síndrome de reservorio irritable, el desarrollo de abscesos y fístulas, la disfunción sexual (dispareunia en hasta un 26% de los casos, impotencia en un 1,5%), infertilidad por adherencias en las trompas de Falopio (el riesgo se triplica).
En resumen, la colectomía es una opción, a veces la única, para los pacientes con CU grave refractaria a corticoides. El hecho de que existan cada vez nuevos fármacos no debe de hacer cambiar los tiempos de plazo de evaluación de la respuesta ni de la necesidad de colectomía. Sus resultados a corto plazo son satisfactorios, dado el estado psicológico de muchos de ellos. Aunque si bien la proctocolectomía y la ileostomía terminal se pueden considerar "curativas", es importante recalcar que no es así con la colectomía, ya que hay una incidencia significativa de complicaciones funcionales a largo plazo en las personas sometidas a AIR.
Conclusiones
Ante un caso de CU refractaria al tratamiento corticoideo a dosis plena el factor más importante para conseguir un resultado exitoso será la buena relación entre el paciente, el digestivo y el coloproctólogo con la finalidad de una actuación adecuada lo más precoz posible. Se establece que se debe de introducir tratamiento inmunosupresor tras tres días sin respuesta a corticoides intravenosos a dosis plena.
Actualmente la evidencia científica y la disponibilidad de nuevos tratamientos inmunosupresores han aumentado la oferta de tratamiento médico antes de tener que recurrir a la colectomía, aceptándose que un paciente pueda recibir dos inmunosupresores distintos antes de recurrir a la cirugía (con un tiempo medio de espera de respuesta de siete días desde el inicio del tratamiento con el inmunosupresor).
La elección por ciclosporina o por infliximab va a depender de la experiencia del digestivo con cada uno de ellos, de la posibilidad de medición de los niveles de ciclosporina en sangre y del antecedente de tratamiento previo con azatioprina (en cuyo caso se optará por infliximab, como ya hemos comentado). Según los datos disponibles actualmente, las tasas de complicaciones posoperatorias no parecen ser más altas en quienes recibieron previamente infliximab o ciclosporina con corticoides[48], sin embargo existe un estudio que informó de una tasa de complicaciones del 80% en un paciente tratado con dos inmunosupresores seguidos (ciclosporina y corticoides seguido de infliximab)[49].
En el caso de optar por la ciclosporina, se recomienda una terapia inicial de tres días con ciclosporina intravenosa a dosis baja (2 mg/kg peso/día) seguido (si ha habido respuesta) de ciclosporina oral (por no más de tres meses) más tratamiento concomitante con azatioprina/6MP.
En el caso de usar infliximab se optará por al menos un tratamiento de inducción de 5 mg/kg peso en las semanas 0,2 y 6.