CORRESPONDENCIA
Ángel Caunedo-Álvarez
Unidad de Gestión Clínica de Aparato Digestivo
Hospital Universitario Virgen Macarena
Av Dr Fedriani s/n. 8ª Planta. 41071 Sevilla.
Tlf 955008801 - Fax 955008805.
acaunedoa@gmail.com
Introducción, definición y perspectiva histórica
Los eosinófilos fueron descritos hace más de un siglo como células blancas sanguíneas granulocíticas marcadamente acidófilas y por tanto con intensa afinidad por la tinción con eosina. Estas células proceden de la médula ósea y desde allí son transportados por el torrente sanguíneo hacia ciertos tejidos, fundamentalmente la lámina propia del tracto digestivo (con excepción del esófago, donde no residen en condiciones fisiológicas)[1]. La función de los eosinófilos es mantener el necesario equilibrio que permita la defensa del tracto gastrointestinal ante sustancias tóxicas externas, mediante la modulación del sistema inmune, y la absorción eficiente de los nutrientes ingeridos[2], [3].
La existencia de ciertos estímulos que incluyen agresiones tisulares inespecíficas, infecciones (especialmente parasitarias) y alérgenos, provocan la liberación, por parte de mastocitos y células Th2, de una serie de citoquinas (IL5, IL13, IL4, TNF) que promueven el reclutamiento y la activación de los eosinófilos[4], [5]. Tras su activación, los eosinófilos incrementan su producción de IgE y de citoquinas y liberan numerosas sustancias (Tabla 1) con funciones inflamatorias, citotóxicas, vasoconstrictoras, neuromoduladoras y quimiotácticas[6], por lo que no sólo se trata de células efectoras sino inmunorreguladoras en el amplio sentido del término[7].
Tabla 1
Sustancias liberadas tras la degranulación de los eosinófilos.
La patología causada por la disfunción de los eosinófilos en el tracto digestivo incluye, en su concepción más extensa, tanto trastornos secundarios (debidos a alguna de las numerosas causas de eosinofilia) como primarios (aquellos en los que dichas causas son excluidas). Del mismo modo, pueden observarse manifestaciones digestivas por eosinofilia tisular en aquellos casos de síndrome hipereosinofílico general que cursa también con afectación gastrointestinal. Sin embargo, cuando hablamos de enfermedades gastrointestinales por eosinófilos (EGE) hacemos referencia al grupo de trastornos causados por el infiltrado de eosinófilos maduros a cualquier nivel del tracto digestivo, de causa primaria, en el que se ha excluido cualquier afectación extradigestiva (descartándose así el mencionado síndrome hipereosinofílico). Atendiendo al órgano afectado, dentro de las enfermedades eosinofílicas gastrointestinales se incluyen la esofagitis eosinofílica, la gastroenteritis eosinofílica, la colitis eosinofílica, la colecistitis eosinofílica y la pancreatitis eosinofílica.
Desde una perspectiva histórica, puede decirse que EGE fueron inicialmente descritos en 1937 por Kaijser[8], si bien esta entidad fue escasamente estudiada hasta que Klein, en 1970, publicó una serie de 7 nuevos casos, y en una completa revisión de la literatura definió los tres patrones clínicos relacionados con la capa histológica principalmente afectada[9]. Posteriormente, en 1984, Oyaizu y cols describieron el mecanismo de quimiotaxis de los eosinófilos en la gastroenteritis Eosinofílica (GE), que estaría mediado por los mastocitos e inducida por IgE[10]. Posteriormente, Talley en 1990 publicó la primera gran serie de pacientes con GE, un total de 40, siguiendo los patrones clínicos propuestos por Klein[11]. Desde esa fecha, el número de publicaciones sobre la patología gastrointestinal por eosinófilos ha crecido exponencialmente, hasta el punto de que sólo entre 2006 y 2008 se publicaron casi 500 artículos relacionados con el tema.
Aspectos etiopatogénicos
La etiopatogenia de las EGE no es del todo conocida, si bien varias revisiones sobre este aspecto han sido publicadas en los últimos años con la intención de unificar algunas de las hipótesis propuestas[12], [13]. La mayoría de los autores reconocen la intervención de una etiología alérgica en la mayoría de los pacientes, basándose en dos hechos fundamentales, por una parte que el 50-75% de pacientes con EGE son atópicos (muchos de ellos con elevación de IgE específica para alérgenos alimentarios), y por otra, que los mediadores característicos de la EGE (células y citoquinas Th2, eotaxinas y mastocitos) han sido implicados también en otras enfermedades alérgicas[14]-[16].
Sin embargo, los artículos iniciales en los que se describían pequeñas series de pacientes demostraban escaso o nulo beneficio clínico tras la retirada de los denominados "alimentos desencadenantes" en aquellos casos con historia de alergia alimentaria[9], [17]. En esta misma línea, varios estudios igualmente clásicos no pudieron identificar una reacción alérgica reproducible en todos los pacientes, y la mayaría de los enfermos con GE mostraban una respuesta normal a mitógenos habituales como la fitohemaglutinina[18]. En cualquier caso, la hipótesis más ampliamente aceptada sugiere que las citoquinas de la respuesta Th2, producidas bien por la vía dependiente de IgE, bien por la vía de células T, serían las responsables de la eosinofilia tisular gastrointestinal[19]. Hasta la fecha no se ha podido determinar si alguna de estas vías tiene un papel dominante o si las EGE son realmente un desorden mixto.
Independiente de su procedencia, las citoquinas expresadas en las EGE (como la IL-4, IL-5 e IL13) producen una serie de eventos que desembocan en la inflamación del tejido[20]. En este proceso, la IL-4 juega un papel dominante en la retroalimentación positiva de la diferenciación Th2, mientras que IL4 e IL-13 son esenciales para la expresión de IgE. La IL-5, por su parte, es la citoquina eosinofílica más activa in vivo, estimulando procesos como la producción, liberación desde la médula ósea, activación y supervivencia de los eosinófilos[21]. La función principal de la IL-13 en el proceso parece ser la de efector inflamatorio, ya que estimula la producción de citoquinas como la CCL-26 (eotaxina-3) y células de adhesión (VCAM), potenciando así el proceso inflamatorio[22]. Numerosos estudios han demostrado además el papel central que parece desempeñar la eotaxina-3 en la esofagitis eosinofílica, habiéndose descrito no sólo una sobreexpresión del gen que codifica dicha citoquina en la biopsia esofágica de estos pacientes, sino incluso una correlación directa entre los niveles de dicha molécula y el número de eosinófilos en esófago[23].
En cualquier caso, bajo la denominación de EGE, probablemente coexistan varios subgrupos clínicos y fisiopatológicos específicos (esofagitis eosinofílica vs GE; entidades alérgicas vs no alérgicas, etc…), cada uno de los cuales con diferencias más o menos importantes en sus vías etiopatogénicas iniciales aún cuando puedan compartir una vía efectora final común.
Epidemiología y clínica
Aunque todos los autores coinciden en señalar que la GE es una entidad poco frecuente, existen pocos datos sobre su prevalencia y distribución geográfica. En una revisión de casos entre 1966 y 2003, Álvarez y cols[24] encontraron menos de 300 casos publicados en todo el mundo, de los que 51 correspondían a España. Talley y cols[11], en una revisión ya clásica, comunicaron 40 casos procedentes del registro general de la Clínica Mayo entre 1950 y 1987, sobre un total de 4 millones de enfermos atendidos, lo que supondría aproximadamente 1 caso por cada 100.000 pacientes en centros de referencia. Algunos autores sospechan sin embargo, que la prevalencia podría ser superior y que una proporción no desdeñable de casos se encontraría infradiagnosticada, por lo que un elevado grado de sospecha podría elevar las mencionadas cifras[25]-[27].
La GE puede afectar a cualquier grupo de edad, habiéndose reportado casos tanto en niños como en ancianos[28], si bien parece existir un pico de incidencia entre la 3º y 5º década de la vida[29], [30]. Parece existir además una ligera predominancia en el sexo masculino (1.4:1)
Guajardo y cols, en un registro mundial a través de una página web, encuentra que en el 80% de los 57 casos con GE comunicados existía una condición atópica conocida, e incluso el 62% de los pacientes presentaba alguna alergia alimentaria[31]. No obstante, el registro es una iniciativa desarrollada por pediatras, siendo la edad media de los pacientes incluidos con EGE de 15 años, y es posible que el porcentaje de atopia y alergia alimentaria sea menor entre pacientes adultos.
La gastroenteritis eosinofílica se clasifica de acuerdo con el predominio de infiltración eosinofílica en las diferentes capas de la pared intestinal (Klein clasificación): formas mucosa, muscular y serosa[9], aunque a menudo las características clínicas se superponen ya que pueden estar afectadas varias capas[11]. Las manifestaciones clínicas dependen de la profundidad y de las capas afectadas, y el rango de los síntomas abarca desde una clínica apenas perceptible hasta la desnutrición, la obstrucción intestinal o la ascitis eosinofílica[11]-[34]. Tal como se demuestra en una revisión clínica de 220 casos, el estómago y el intestino delgado proximal son las localizaciones más frecuentes de la GE, mientras que un tercio de los pacientes presentaron afectación en más de una localización[35].
La forma mucosa es probablemente la más común (55-58%), seguida por la muscular (30%) y por último la serosa (12.5%). La GE con predominio de afectación mucosa es la presentación en la que se ha visto una mayor relación de antecedentes alérgicos (hasta en el 50% de los pacientes), y se manifiesta como dolor abdominal, náuseas, vómitos, diarrea, anemia por deficiencia de hierro, a veces con hematoquecia y enteropatía pierde-proteínas, lo que puede conducir en el niño a fallo de medrar y en adultos a pérdida de peso y desnutrición[30,35], [36]. En la afectación principalmente muscular se observa un marcado engrosamiento de la pared gástrica o intestinal que puede conducir a cuadros suboclusivos o en último término a una obstrucción completa[37]-[42]. La forma serosa es la más inusual, y su principal manifestación es la ascitis eosinofílica (con una disminución en el gradiente de albúmina suero: ascitis), que a menudo se acompaña de derrame pleural, intensa eosinofilia periférica y en ocasiones características de peritonitis[11], [43], [44].
Además de las mencionadas manifestaciones de la eosinofilia en el tracto gastrointestinal, se han descrito otras presentaciones más inusuales como las úlceras pépticas complicadas[45]-[49] o la perforación intestinal, a las que habría que añadir las formas biliares, como la colecistitis eosinofílica[26] y la colangitis eosinofílica[50] o la afectación pancreática, que puede manifestarse como nódulo pancreático[51]-[53] o como pancreatitis aguda[54]-[56]. Se han descrito igualmente casos anecdóticos de hepatopatía asociada a infiltración eosinofílica, habitualmente en el contexto de un síndrome hipereosinofílico general[57], [58].
Diagnóstico
Los criterios diagnósticos que definen la GEE son la presencia de síntomas gastrointestinales, la infiltración por eosinófilos de una o más áreas gastrointestinales demostradas por biopsia y la exclusión de otras causas de eosinofilia tisular[11].
Para establecer el diagnóstico de la GE es preciso un elevado nivel de sospecha clínica, ya que los síntomas no son específicos. El diagnóstico suele demorarse especialmente en los pacientes con formas leves en los que sólo existe clínica sutil, o bien en las formas con escasa afectación mucosa, en las que la biopsia endoscópica no es concluyente.
Las pruebas de laboratorio en estos pacientes suelen mostrar las alteraciones propias de un estado inflamatorio (reactantes de fase aguda), a las que puede sumarse una hipoproteinemia variable en los casos de afectación mucosa severa con enteropatía pierde-proteínas[59]. Aunque la eosinofilia periférica es frecuente en estos enfermos, puede ser normal en más del 25% de los casos[11], [60], [61]. En un estudio recientemente publicado por Lee y cols[62] con 39 pacientes diagnosticados de GE, aquellos con una eosinofilia periférica muy elevada (mayor de 1500 eos/mcl) presentaron mayor tasa de atopia, afectación de segmentos más extenso de intestino así como mayor riesgo de trombosis. Otros hallazgos como la elevación sérica de IgE e IL-5 en suero o en líquido ascítico se han propuesto como útiles para orientar el diagnóstico, especialmente en la edad pediátrica. En presencia de ascitis la paracentesis diagnóstica para determinación de eosinófilos en líquidos ascítico tiene gran rendimiento diagnóstico[63].
El estudio detallado de parásitos en heces (incluyendo Ascaris, Anisakis, Ancylostoma, Strongyloides, Capillaria, Toxicara, Trichiuria and Trichinella) es preciso en estos pacientes ya que la parasitosis intestinal es causa relativamente frecuente de eosinofilia, especialmente en áreas endémicas[64]-[67].
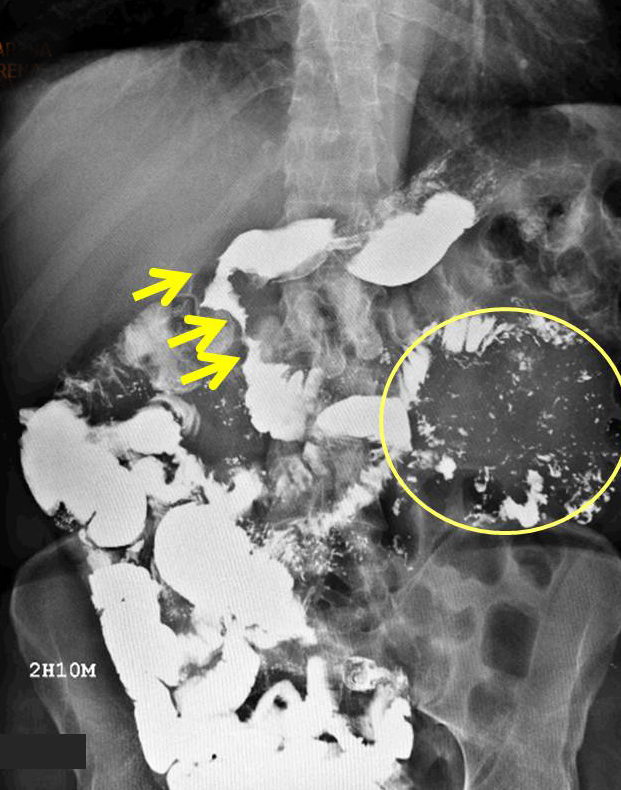
Radiológicamente, la gastroenteritis eosinofílica no tiene unas características específicas. Los cambios radiológicos son variables o ausentes en al menos el 40% de los pacientes (68). Los estudios baritados (Figura 1), la ecografía y el TAC abdominal (Figura 2) pueden mostrar engrosamiento de las paredes intestinales o signos de obstrucción en las formas con mayor afectación de la capa muscular, así como linfadenopatía localizada en algunas ocasiones[69], [70]. Del mismo modo, en los casos de afectación bilio-pancreática, tanto el TAC como la ecografía o la RNM (Figura 3) pueden mostrar dilatación de vías biliares y/o pancreáticas[71], [73], hallazgos propios de una pancreatitis aguda[74], o masas pancreáticas de características hipoecóicas/hipodensas[51]-[53]. Algunos estudios consistentes en pequeñas series de casos han sugerido el papel de la exploración con Tc-99m HMPAO en la detección de inflamación activa en la gastroenteritis eosinofilica, especialmente en la evaluación de la extensión de la enfermedad y la respuesta al tratamiento, si bien no serviría para identificar la causa de la inflamación detectada[75], [76].
Figura 1
Tránsito intestinal en un paciente con GE en el que se observa un marco duodenal con estenosis irragulares (flechas amarillas), así como un área (círculo) con floculación y cierta fragmentación del contraste (caso propio).
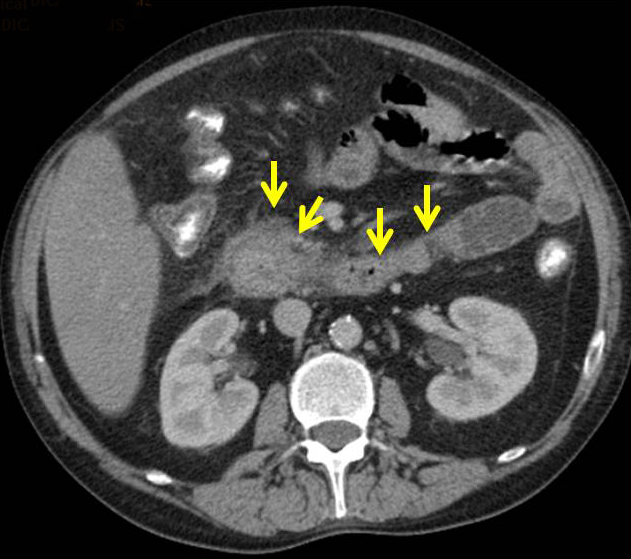
Figura 2
Imagen de TAC de un paciente con engrosamiento de las paredes de duodeno (flechas amarillas) que causa áreas de estenosis (caso propio).
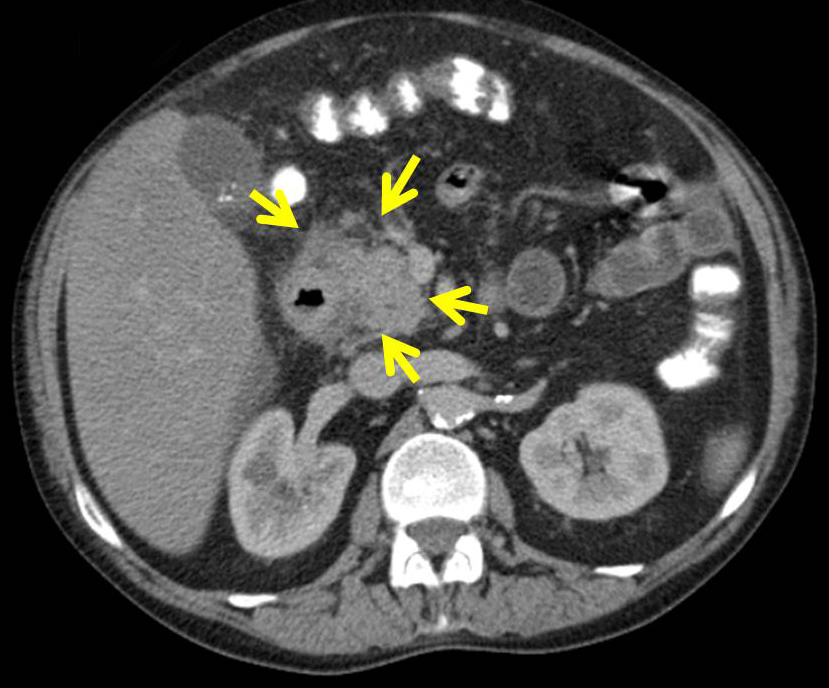
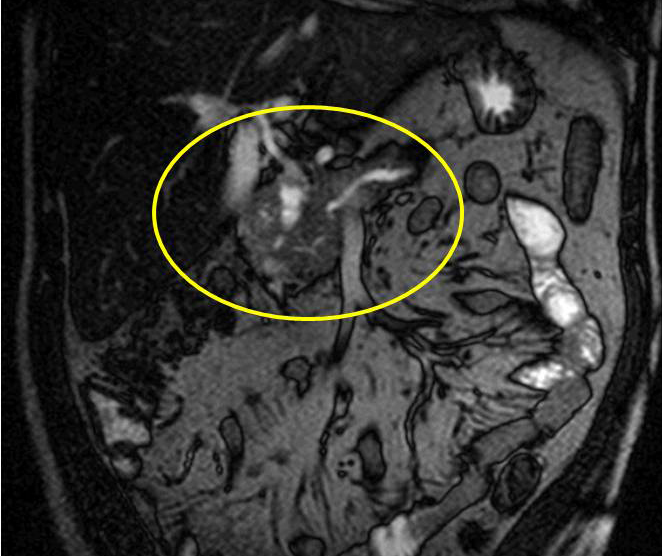
Figuras 3A y 3B
Paciente con Gastroenteritis y Pancreatitis Eosinofílica, manifestada como masa en cabeza de páncreas visible en TAC abdominal (3A) y RNM de abdomen (3B) (caso propio).
La endoscopia digestiva con biopsia de estómago y duodeno es sin duda el procedimiento más rentable en la GE con afectación mucosa, ya que gracias a su capacidad de obtener muestras logra el diagnóstico en un 80% de casos. En los casos de afectación exclusivamente intestinal puede ser necesario realizar una enteroscopia (por pulsión, o bien de doble/simple balón) para identificar el área afectada y tomar muestras (Figura 4). Los hallazgos endoscópicos son inespecíficos y muy variables, e incluyen desde un aspecto prácticamente normal hasta engrosamiento de pliegues, eritema, friabilidad, nodularidad, erosiones, úlceras, exudado o estenosis[77]-[79]. Durante la endoscopia es importante tener en cuenta que la toma de biopsias debe realizarse sobre cualquier alteración mucosa pero también sobre la mucosa de aspecto normal, ya que ésta puede albergar infiltración eosinofílica. La infiltración eosinofílica puede ser parcheada, lo que hace aconsejable tomar al menos 4-5 muestras tanto del estómago como del intestino delgado[27]. Esta naturaleza a veces parcheada de la afectación hace que la ausencia de eosinófilos en una muestra endoscópica concreta no excluye el diagnóstico de GE. Recientemente, han sido publicados algunos casos de GE en los que mediante el estudio con cápsula endoscópica se describen los hallazgos mucosos más característicos (Figura 5) o se identifican estenosis previamente no conocidas[80]-[83], si bien, debido a su incapacidad para tomar biopsias y lo inespecífico del aspecto endoscópico de la enfermedad, su utilidad hoy día para esta indicación no está establecida. En este mismo sentido, Endo y cols a partir de un caso anecdótico, proponen la cápsula endoscópica como procedimiento no invasivo para comprobar la eficacia del tratamiento sobre la mucosa intestinal[84].
Figura 4
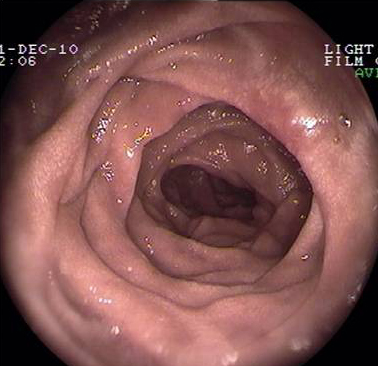
Imagen obtenida de una enteroscopia realizada a un paciente con GE de afectación predominantemente mucosa, en la que se observa cierto aspecto atrófico y áreas denudadas. La biopsia demostró una intensa infiltración eosinofílica (caso propio).
Figura 5
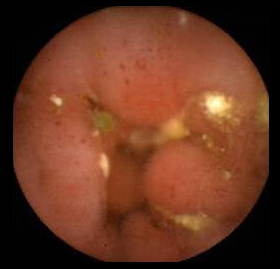
Pliegues edematosos, punteado petequial y algunas pequeñas erosiones vistas por cápsula endoscópica en paciente con GE (caso propio).
Las formas de GE con afectación primordialmente muscular requieren con frecuencia la biopsia quirúrgica de la pared intestinal completa o la resección para llegar al diagnóstico definitivo, ya que una escasa o nula afectación mucosa hace no concluyente la toma de muestra endoscópica[85]-[87]. Se han publicado casos anecdóticos de biopsias por punción dirigidas por ecografía en casos de afectación exclusivamente muscular, sin embargo este procedimiento no ha sido refrendado por otros autores[88]. En cuanto a la GE con afectación serosa, aunque en ocasiones la biopsia peritoneal por vía laparoscópica puede ser necesaria[43], habitualmente el contexto clínico-analítico, una marcada eosinofilia en el líquido ascítico y una rápida respuesta al tratamiento corticoideo confirman el diagnóstico[63], [89].
La demostración en el estudio histológico de eosinofilia tisular en el tracto gastrointestinal de un paciente con un contexto clínico-analítico compatible en el que se han descartado otras causas de eosinofilia permite establecer el diagnóstico de GE. Sin embargo, es preciso señalar algunas limitaciones a considerar en el estudio anatomo-patológico de estos pacientes. En primer lugar, el grado de experiencia del patólogo puede ser importante en el reconocimiento de la enfermedad, si bien hasta la fecha no existen estudios sobre el error intra e interobservador en la interpretación de las biopsias de pacientes con EGE. En segundo lugar, a diferencia de lo que ocurre en el esófago, en estómago e intestino puede ser normal la presencia de eosinófilos en la mucosa, y es el incremento en el número lo que permite establecer la alteración. En este sentido, la mayoría de los autores consideran significativa una cantidad por encima de 30 eos/cga en estómago[90] y de 20-25 eos/cga en intestino[91]-[93]. En tercer lugar, es importante resaltar que el método de fijación utilizado puede ser un aspecto crítico en la definición de los eosinófilos en biopsias gástricas e intestinales. La solución de Bouin, a menudo utilizada para muestras gastrointestinales, puede causar un "blanqueamiento" de los gránulos de eosinófilos, haciendo mucho más difícil la detección[94]. Por ello, ante la sospecha de GE, se recomienda utilizar la fijación en formol, que ha demostrado su capacidad para proporcionar más material óptimo para la tinción[95]. Además de la infiltración eosinofílica en la lamina propia, se han descrito otros hallazgos histológicos que pueden verse en pacientes con GE, tales como la presencia de eosinófilos en la criptas intestinales y las glándulas gástricas, la hiperplasia de criptas, la necrosis de células epiteliales, la atrofia vellositaria, el infiltrado mastocitario o la hiperplasia de ganglios linfáticos mesentéricos por infiltración eosinofílica[16]-[85].
Los criterios que permiten establecer el diagnóstico de GE (se exige el cumplimiento de todos ellos) son: a) la presencia de síntomas gastrointestinales, b) la demostración histológica de una infiltración eosinofílica en una o más áreas gástricas y/o intestinales (algunos autores aceptan en su lugar, en los casos de afectación muscular, la presencia de hallazgos radiológicos compatibles junto con eosinofilia periférica), y c) la exclusión de otras causas de eosinofilia[11], [36], [96]. Resulta pues esencial el diagnóstico diferencial con otras causas de eosinofilia tisular y/o periférica entre las que se incluyen las infestaciones por helmintos, la infección por H Pylori, las vasculitis, ciertas conectivopatías, la hipersensibilidad a fármacos, algunos casos de enfermedad inflamatoria intestinal y determinadas enfermedades hematológicas malignas (Tabla 2). Entre este último grupo cabe destacar el síndrome hipereosinófilo, enfermedad mieloproliferativa caracterizada por una eosinofilia periférica superior a 1500 cel/gl, y la presencia de eosinofilia tisular en varios órganos, habitualmente corazón, pulmones, cerebro y riñones. Esa afectación multivisceral, así como la alteración en los valores de vitamina B12 y de triptasa sérica en mastocitos, o más recientemente la demostración de la anomalía genética subyacente (fusión del gen Fip1-like1 + gen PDGFR por delección), permiten establecer su diagnostico diferencial con la GE[16], [97], [98].